Skillnad mellan geometriska isomerer och strukturella isomerer
Geometriska isomerer vs strukturella isomerer
Isomerer är olika föreningar med samma molekylformel. Det finns olika typer av isomerer. Isomerer kan huvudsakligen delas in i två grupper som konstitutionella isomerer och stereoisomerer. Konstitutionella isomerer är isomerer där atomernas anslutning skiljer sig åt i molekyler. I stereoisomerer är atomer anslutna i samma sekvens, till skillnad från konstitutionella isomerer. Stereoisomerer skiljer sig endast i arrangemanget av sina atomer i rymden. Stereoisomerer kan vara av två typer, enantiomerer och diastereomerer. Diastereomerer är stereoisomerer, vars molekyler inte är spegelbilder av varandra. Enantiomerer är stereoisomerer, vars molekyler är nonsuperposibla spegelbilder av varandra. Enantiomerer förekommer endast med kirala molekyler. En chiral molekyl definieras som en som inte är identisk med sin spegelbild. Därför är den kirala molekylen och dess spegelbild enantiomerer av varandra. Till exempel är 2-butanolmolekylen chiral, och den och dess spegelbilder är enantiomerer.
Geometriska isomerer
Geometriska isomerer är en typ av stereoisomerer. Denna typ av isomerer resulterar, när molekyler har en begränsad rotation, i grunden på grund av en dubbelbindning. När det finns en enda kol-kolbindning är rotationen möjlig. Därför ritar vi atomer, deras arrangemang kommer att vara desamma. Men när det finns en kol-kol dubbelbindning kan vi rita två arrangemang av atomer i en molekyl. De resulterande isomererna är kända som cis-, trans-isomerer eller E-Z-isomerer. I cis-isomer finns samma typer av atomer på samma sida av molekylen. Men i trans-isomeren finns samma typer av atomer i motsatta sidan av molekylen. Exempelvis är cis- och transstrukturerna för 1,2-dikloretan som följer.
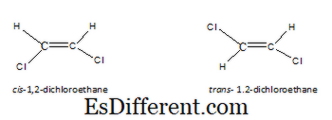
För att en molekyl ska ha geometriska isomerer är det inte bara tillräckligt att endast ha en dubbelbindning. De två atomer eller grupper som är fästa vid ena änden av dubbelbindningen bör vara olika. Till exempel, efter molekylen har inte geometriska isomerer, båda atomerna i vänstra änden är hydrogener. På grund av det, om vi ritar det i antingen cis eller trans, är båda molekylerna desamma.

Men det spelar ingen roll om alla fyra bifogade grupper eller atomer är olika. I det tillfället kan vi namnge dem som E eller Z.
Strukturisomerer
Dessa kallas också konstitutionella isomerer. Konstitutionella isomerer är isomerer, där atomernas anslutning skiljer sig åt i molekyler. Butan är den enklaste alkanen för att visa konstitutionell isomerism. Butan har två konstitutionella isomerer, butan själv och isobuten.

Eftersom deras kopplingar är olika har två molekyler olika fysikaliska och kemiska egenskaper.Strukturisomerer kan bildas av kolväten där de har minst fyra kolatomer. Det finns tre typer av strukturella isomerer som skelett, positionella och funktionella gruppisomerer. I skelettisomerismen, som ges i det ovanstående exemplet, omorganiseras skelettet för att ge olika isomerer. I position isomerer ändras en funktionell grupp eller en annan grupp position. I funktionella gruppisomerer, även om de har samma formel, skiljer sig molekylerna från att ha olika funktionella grupper.
|
Vad är skillnaden mellan Geometric Isomers och Structural Isomers ? • Geometriska isomerer är stereoisomerer. Därför är anslutningsförhållandena samma i jämförelse med strukturella isomerer, där isomerer skiljer sig på grund av atomernas anslutningar. I geometriska isomerer skiljer sig de på grund av det tredimensionella arrangemanget i utrymmet. • Ofta för en molekyl finns två geometriska isomerer som cis, trans eller E, Z, men för en molekyl kan det finnas ett stort antal strukturella isomerer. • Geometrisk isomeri visas i grunden av molekylen med kol-kol-dubbelbindningar. Strukturisomerism visas också av alkaner, alkener, alkyner och aromatiska föreningar. |



