Skillnad mellan kombination och sönderdelning reaktion | Kombination vs sönderdelningsreaktion
Huvudskillnad - Kombination vs sönderdelningsreaktion
En kemisk reaktion är omvandlingen av en eller flera kemiska föreningar till en eller flera olika produkter, förändra identiteten för en kemisk förening. Utgångsmaterialet för en kemisk reaktion kallas reaktanten och den resulterande föreningen kallas produkten. Fördelning av föreningar eller kombination av föreningar och bildning av nya föreningar kommer att inträffa under en kemisk reaktionsprocess eftersom bindningarna mellan föreningarna av atomer är brutna och skapade på ett annat sätt. Kemiska reaktioner kan delas upp i flera stora kategorier. Redoxreaktioner eller oxidations-reduktionsreaktioner är mycket viktiga bland dem. Oxiderings- och reduktionsreaktionerna kallas elektronöverföringsreaktioner eftersom elektronerna av reaktanter överförs från en förening till den andra för att orsaka reaktionen. I redoxreaktioner uppträder två parallella reaktioner, som kallas halveraktioner, samtidigt. Dessa halva reaktioner visar överföringen av elektroner. Genom att balansera dessa halvreaktioner kan man gissa den övergripande reaktionen som har hänt i slutet. Kombinationsreaktioner och sönderdelningsreaktioner är två huvudtyper av redoxreaktioner. Huvudskillnaden mellan kombination och sönderdelningsreaktion är att kombinationsreaktion involverar en kombination av reaktanter för att ge en enda produkt medan sönderdelningsreaktion involverar nedbrytningen av en enda förening i två eller flera produkter.
INNEHÅLL
1. Översikt och nyckelfaktor
2. Vad är en kombinationsreaktion
3. Vad är en nedbrytningsreaktion
4. Jämförelse vid sida vid sida - Kombination mot nedbrytningsreaktion
5. Sammanfattning
Vad är en kombinationsreaktion?
En kombinationsreaktion, även kallad syntesreaktion , är en reaktion i vilken reaktantföreningar kombineras för att bilda en annan förening som produkten. Med andra ord resulterar reaktionen av enkla molekyler i en komplex molekyl. Några eller alla bindningarna mellan atomer av den specifika föreningen är nedbrutna; samtidigt kommer atomer att kombinera för att bilda den nya föreningen, vilken är produkten. I sönderdelningsreaktioner fungerar samma reaktant som utgångsmaterial för båda halva reaktionerna.Till skillnad från i sönderdelningsreaktioner börjar de halva reaktionerna i kombinationsreaktionerna till att börja med olika reaktanter. Kombinationsreaktion resulterar i en enda produkt. Följande är ett vanligt exempel som kan ges som förbränningsreaktioner.
När aluminium (Al) placeras i flytande bromid (Br2 ) uppträder en kombinationsreaktion och producerar aluminiumbromid (AlBr 3 ). Här ökas oxidationsnumret i Al och minskar i Br. Därför är det en redoxreaktion och är en kombinationsreaktion eftersom två reaktanter har reagerat för att ge en viss produkt. Figur 01: Kombinationsreaktion
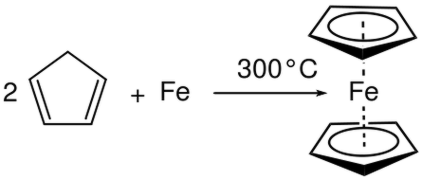
Nedbrytningsreaktion är en annan viktig reaktion i kategorin av redoxreaktioner. Det är i grunden motsatt av kombinationsreaktionen. En sönderdelningsreaktion är en reaktion där reaktantföreningen är uppdelad i produkter. Här uppträder halvreaktioner samtidigt som oxidationsreaktionen och reduktionsreaktionen. Men till skillnad från i kombination reaktion är reaktanten för båda halva reaktionerna densamma i sönderdelningsreaktioner. Nedbrytningsreaktion resulterar i flera produkter.
Vid elektrolys av vatten sönderfaller vattenmolekylerna för att ge syre och vätegaser när likström passerar genom vatten. Här ökas oxidationsnumret i syreatom och minskar i väteatom. Därför är det en redoxreaktion och en sönderdelningsreaktion på grund av nedbrytningen av vattenmolekyler i syre och vätegaser.
Figur 02: Kombination vs sönderdelning

Vad är skillnaden mellan Kombinations- och sönderdelningsreaktion?
- diff Artikel Middle before Table ->
Kombination vs sönderdelningsreaktion
Två eller flera reaktantföreningar är involverade i kombinationsreaktioner. |
|
| En enda förening är involverad i en sönderdelningsreaktion. | Produkter |
| Kombinationsreaktion resulterar i en enda produkt. | |
| Nedbrytningsreaktioner resulterar i flera produkter. | Halva reaktioner |
| I kombinationsreaktioner har två halva reaktioner två olika utgångsmolekyler. | |
| I sönderdelningsreaktioner fungerar en enda molekyl som utgångsmaterial för båda halva reaktionerna. | Kemiska bindningar |
| Kombinationsreaktioner resulterar i bindning av atomer för framställning av den enda ändprodukten. | |
| I sönderdelningsreaktioner bryts kemiska bindningar ned för att bilda två eller flera slutprodukter. | Molekyler |
| Kombinationsreaktioner gör att enkla molekyler reagerar och producerar komplexa molekyler. | |
| Nedbrytningsreaktioner orsakar komplexa molekyler att bryta ner i enkla molekyler. | Sammanfattning - Kombination vs sönderdelning Reaktion |
Redoxreaktioner är mycket en del av världen runt omkring oss eftersom majoriteten av de viktiga kemiska reaktionerna är redoxreaktioner. Kombinationsreaktioner och sönderdelningsreaktioner är enkla reaktioner som är motsatta av varandra. Huvudskillnaden mellan kombination och sönderdelningsreaktion är att kombinationsreaktionen involverar kombinationen av två eller flera reaktantmolekyler för att resultera i en enda slutprodukt medan sönderdelningsreaktion involverar nedbrytning av en enda molekyl i två eller flera produkter.
Referenser:
1. Chang, R., 2010. kemi. 10: e upplagan. NewYork: McGraw-Hill.
2. Redox. (2009, 30 juli). Hämtad 29 maj 2017, från // svaginteraktioner. wordpress. com / primrar / redox /
3. Reaktioner. (n. d.). Hämtad 29 maj 2017, från // www. ric. edu / fakultet / ptiskus / reaktioner /
Image Courtesy:
1. "Miller Ferrocen Synthese" av Bert. Kilanowski - eget arbete (CC0) via Commons Wikimedia
2. "Kemiska reaktioner" Av Daniele Pugliesi - Egent arbete (CC BY-SA 3. 0) via Commons Wikimedia [Beskurna]




